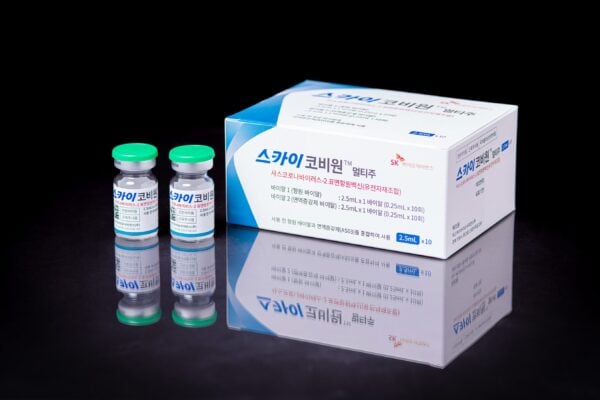
La vacuna SKYCovion COVID-19, desarrollada en Corea del Sur con 3,6 millones de dólares en financiación de la Fundación Bill y Melinda Gates, recibió recientemente la aprobación regulatoria de la Agencia Reguladora de Medicamentos y Productos Sanitarios (MHRA) del Reino Unido.
«SK bioscience, una empresa global innovadora de vacunas y biotecnología comprometida con la promoción de la salud humana desde la prevención hasta la cura, ha anunciado hoy que la Agencia Reguladora de Medicamentos y Productos Sanitarios (MHRA) del Reino Unido ha concedido la Autorización de Comercialización (MA) para la vacuna COVID-19 de SK bioscience SKYCovion™ (nombre de marca en
Una vez que una vacuna recibe la autorización de comercialización, se puede comercializar y distribuir al público.
Se convierte en la octava vacuna contra la COVID-19 autorizada por el regulador independiente de medicamentos del Reino Unido.
SKYCovion es una vacuna de nanopartículas, que utiliza una pieza de la proteína pico del virus SARS-CoV-2 junto con la tecnología adyuvante AS03 de GlaxoSmithKline, «un ingrediente adicional diseñado para desencadenar una respuesta inmune más fuerte».
La vacuna supuestamente cumplió con los estándares de seguridad, calidad y eficacia requeridos establecidos por la MHRA. Esta aprobación ha provocado preocupaciones de varios científicos, en particular el profesor británico Norman Fenton, según SLAY News.
La MHRA ha señalado que la duración de la protección ofrecida por la vacuna SKYCovion sigue siendo desconocida, y no se espera ninguna protección después de la dosis inicial. Además, actualmente no hay datos sobre su seguridad y eficacia para personas inmunodeprimidas.
Tampoco hay investigaciones sobre sus efectos en las mujeres embarazadas o si la vacuna se excreta en la leche materna. El folleto informativo del paciente indica que la vacuna no debe administrarse a mujeres embarazadas o amamantando.
Hasta la fecha, SKYCovion no se ha sometido a ningún estudio de carcinogenicidad o genotoxicidad, ni se ha probado la intercambiabilidad con vacunas de otros fabricantes. Si bien la vacuna ha sido autorizada para la autorización condicional para los mayores de 18 años, el profesor Fenton está presionando por la transparencia, presentando una solicitud de libertad de información a la directora ejecutiva de MHRA, June Raine.
A pesar de estas incertidumbres, se informa que la vacuna se está ofreciendo a personas que han recibido previamente múltiples vacunas contra la COVID-19, según el profesor Fenton. Esto es alarmante, ya que el folleto informativo para el paciente especifica que se requieren dos dosis de la vacuna SKYCovion, con un intervalo de 28 días entre las dosis. No se espera eficacia hasta al menos 14 días después de la segunda dosis.
SLAY News informó citando la guía de la MHRA:
Duración de la protección
Se desconoce la duración de la protección que ofrece la vacuna, ya que todavía se está determinando en los ensayos clínicos en curso.
Personas inmunocomprometidas
La eficacia, la seguridad y la inmunogenicidad de la vacuna no se han evaluado en individuos inmunodeprimidos, incluidos los que reciben terapia con inmunosupresores.
Limitaciones de la eficacia de la vacuna
Según los datos de inmunogenicidad en sujetos naïgenos al SARS-CoV-2, no se prevé ninguna protección después de la primera dosis de la vacuna y es posible que los individuos no estén completamente protegidos hasta 14 días después de su segunda dosis. Al igual que con todas las demás vacunas, es posible que SKYCovion no proteja a todos los receptores de vacunas. La eficacia no se evaluó como parte del programa de ensayos clínicos.
No se ha estudiado la administración concomitante con otras vacunas.
Embarazo
No hay experiencia con el uso de SKYCovion en mujeres embarazadas en ensayos clínicos.
Lactancia materna
Se desconoce si SKYCovion se excreta en la leche humana
Fenton expresó su preocupación por la aprobación de la vacuna, citando la falta de datos de seguridad y la necesidad de más estudios.
Sin embargo, la Comisión Europea está considerando la posibilidad de un despliegue más amplio para el uso público en todas las naciones de la UE, a pesar de las preocupaciones planteadas.
SLAY News informó que una investigación en julio de 2021 encontró que la Fundación Bill y Melinda Gates es el principal financiador de la MHRA, lo que plantea más preguntas sobre posibles conflictos de intereses.
A continuación se muestra el documento de orientación de la MHRA sobre la vacuna no probada:
Fuente: https://www.thegatewaypundit.com/2023/06/here-we-go-bill-gates-funded-covid-vaccine/